何胜洁,毛新亮,张学武
(华南理工大学轻工与食品学院,广东广州 510640)
摘要:本研究以金钱龟肉糜为原料,通过可控的酶解技术制备抗肿瘤活性肽,研究中分别用胰蛋白酶、碱性蛋白酶、木瓜蛋白酶和复合蛋白酶 protamex 对金钱龟肉糜进行酶解并结合超滤初步分离得到了12 种酶解产物,MTT 实验表明其中胰蛋白酶酶解所得分子量小于3000 u 的多肽 E 其抗肿瘤效果最强,当浓度为 1 mg/m L 时,对人肝癌细胞(Hep G-2)和人乳腺癌细胞(MCF-7)的抑制率分别为 92.95%和 67.08%。将 E 利用 Sephadex G-15 进一步纯化,经 MTT 实验筛选得到两组活性较强的多肽组份 E1 和 E2,对 Hep G-2的抗增殖效果来看 E1(IC50为 77.29 μg/m L)强于阳性对照 5-氟尿嘧啶(IC50为 136.27 μg/m L),对于 MCF-7 的抗增殖效果来看 E2(IC50为 214.17 μg/m L)同样要强于阳性对照 5-氟尿嘧啶(IC50为 245.82 μg/m L)。本研究中,抗肿瘤活性肽首次从金钱龟中分离得出,对于以金钱龟为原料的抗肿瘤药物和保健品的开发具有重要指导意义。
关键词:金钱龟;酶解;分离;纯化;抗肿瘤
文章篇号:1673-9078(2015)10-86-90
DOI: 10.13982/j.mfst.1673-9078.2015.10.015
Study of the Separation, Purification, and Anti-tumor Activities of Peptides
Prepared from Enzymolyzed Cuora trifasciata Meat
HE Sheng-jie, MAO Xin-Liang, ZHANG Xue-wu
(School of Light Industry and Food Sciences, South China University of Technology, Guangzhou 510640, China)
Abstract: Here, mincedCuora trifasciata meat was used as a raw material from which peptides with anti-tumor activities were prepared by controlled enzymolysis. Alcalase, papain, trypsin, and protamex were used to carry out the hydrolysis of minced Cuora trifasciata
meat, and 12 different molecular weight hydrolyzates were obtained after ultrafiltration. A 3-(4,5-dimethythiazol-2-yl)-2,5-diphenyl tetrazolium bromide (MTT)assay showed that hydrolyzate E, produced from tryptic digestion with a molecular weight of <3000u, exhibited the best anti-tumor effect.When the concentration was 1 mg/m L, the anti-proliferation rates of hydrolyzate E against human liver cancer cells (Hep G-2) and human breast cancer cells (MCF-7) were 92.95% and 67.08%, rpesectively. Hydrolyzate E was further purified by Sephadex G-15 gel filtration, and two polypeptide fractions (E1 and E2) with strong activity were selected based on an MTT assay. E1 had a stronger anti-proliferative effect on Hep G-2 cells (IC50= 77.29 µg/m L) than the positive control 5-fluorouracil (IC50 = 136.27 µg/m L), while E2 had a stronger anti-proliferative effect on MCF-7 cells (IC50= 214.17 µg/m L) than the positive control 5-fluorouracil (IC50 = 245.82 µg/m L). In this study, peptides with anti-tumor activity were isolated from Cuora trifasciata for the first time, which will have important implications in the development of anti-tumor drugs and health products using Cuora trifasciata as the raw material.
Key words: Cuora trifasciata; enzymolysis; separation; purification; anti-tumor activity
生物活性肽(Biologically active peptides, BAP)是一种具有特殊生理功能的小分子活性物质,如抗肿瘤、抗菌、抗高血压、抗病毒以及提高免疫力等,这些物质广泛存在于动物、植物以及微生物中。生物活性肽主要有4 种来源,分别为蛋白酶解多肽、微生物发酵代谢多肽[1]、天然活性多肽以及化学合成多肽。
由于近几年来恶性肿瘤发病率的不断提高,而传统的化疗药物不仅毒副作用大而且治疗效果并不理想,因此,生物活性肽凭借其活性高、副作用小、针对性强的优势得到了国内外科研工作者的研究和关注。目前已经从多种生物中提取得到了抗肿瘤活性肽,其中动物来源的活性肽展现了广阔的前景。Hsu[2]等分别用木瓜蛋白酶和蛋白酶XXⅢ酶解金枪鱼肉,分离纯化后得到了两种抗肿瘤活性较好的多肽。这两条多肽对乳腺癌细胞 MCF-7 的 IC50值达到了 8.1 和 8.8 μM。Leng[3]等人通过 Sephadex G-25、FPLC 并结合MALDI -TOF 成功的从壳蛤中分离出了对胃癌细胞BGC-823 有明显抑制作用的分子量为3147 u 活性肽,当肽的浓度为4.0 μg/m L 时其对癌细胞的抑制率达到了 60%。另外还分别从贻贝、泥蚶、海鞘、牡蛎等动物体内得到了抗肿瘤肽[4~7],这些都为以后动物体内抗肿瘤肽的提取奠定了基础。
金钱龟又名三线闭壳龟,对抗癌、解毒、消炎、益肝、补肾效果明显,常被用作保健养颜、防治肿瘤和长寿健体的主药之一。然而,目前对于金钱龟多肽的提取、分离纯化及抗肿瘤方面的研究鲜有报道。本文将针对金钱龟的抗肿瘤效果进行研究,采用分离纯化和活性检测相结合的方法提取抗肿瘤活性多肽。本研究为抗癌药物,抗癌保健品的研发及金钱龟的深加工提供理论依据。
1 材料与方法
1.1 原料
金钱龟(购于江门市新会区金田园渔农发展有限公司),乳腺癌细胞 MCF-7、肝癌细胞 Hep G-2(购于中山大学动物细胞实验室)。
1.2 主要的仪器设备和实验试剂
1.2.1 仪器设备
Savant Modulyod 冷冻干燥器,美国Thermo 公司;Allegra X-22R 高速冷冻离心机,美国 Beckman Coulter 公司;UV2300 紫外分光光度计,上海天美科学仪器有限公司;SW-TJ 水平流净化工作台,苏州市净化设备总厂;DBS-100 自动部分收集器,上海沪西分析仪器厂;HL-2B 恒流泵,上海精科实业有限公司;MCO-17AC CO2培养箱,日本 Sanyo公司;MDF -382E 超低温冰箱,日本Sanyo公司;酶联免疫检测仪,Sunris公司;CK41倒置显微镜,Olympus 公司;超滤杯 MS300、超滤膜,上海摩速科学器材有限公司;LDZX-40BI 自动高压灭菌锅,上海申安医疗器械厂;DHG-9075A 电热恒温鼓风干燥箱,上海益恒实验仪器有限公司。
1.2.2 实验试剂
碱性蛋白酶 37017(1:2.5 U/g)为诺维信公司产品;胰蛋白酶(1:250 U/mg)、木瓜蛋白酶(1:800 U/mg)为广州齐云生物科技有限公司产品;复合蛋白酶protamex(1:120 U/mg)为广州迪鑫多生物科技有限公司产品;新生小牛血清、DMEM 培养基(高糖)、链霉素、青霉素为美国 Gibco公司产品;PBS、二甲基亚砜(DMSO)为美国 Amresco公司产品;MTT为美国Sigma公司产品;Na OH 为分析纯。
1.3 实验方法
1.3.1 总氮含量的测定
称取一定量的金钱龟肉糜,参照国标 GB/T5009.5 -2003,用凯氏定氮法测定金钱龟中蛋白质的含量。
1.3.2 不同酶酶解得多肽[9]以及水解度测定
将整只金钱龟除去内脏洗净后绞成肉糜,准确称取4 份质量相同的肉糜 10 g 置于 50 m L 超纯水中,分别用 4 种酶酶解,胰蛋白酶解条件为:p H=8.0,酶解温度 45 ℃,酶解时间 11 h,酶与底物浓度比(E/S)为 0.24%;碱性蛋白酶解条件为:p H=8.5,酶解温度55 ℃,酶解时间 10 h,酶与底物浓度比(E/S)为 4%;木瓜蛋白酶解条件为:p H=7.0,酶解温度 55 ℃,酶解时间 8 h,酶与底物浓度比(E/S)为 0.5%;复合蛋白酶 protamex 酶解条件为:p H=7.0,酶解温度 45 ℃,酶解时间 8 h,酶与底物浓度比(E/S)为 0.43%。所有的酶解过程中都用 0.05 mol/L 的 Na OH 调节反应体系的 p H 值,并控制 p H 值在 p H±0.05 之内。水解结束后在 85 ℃的水浴中保持 10 min,灭酶。冷却到室温然后在 8000 r/min,4 ℃下离心 30 min 后取上清液,冻干后得到酶解多肽。水解度测定采用 p H-stat[10]方法进行,按式(1)计算水解度(DH)。
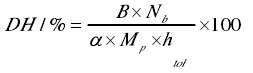 (1)
(1)
tol
式中:B 为碱液体积(m L),Nb为碱液浓度(mol/L),α 为氨基酸的解离度;Mp 为底物中蛋白质的含量/g,htol为底物中蛋白质的肽键总数(mmol/g),参照动物蛋白[11]取 8.60 mmol/g。其中,α、PKα按式(2)和(3)计算(PH 为酶解时的 p H 值,T 为热力学温度/K)。
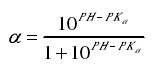 (2)
(2)
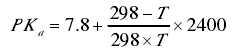 (3)
(3)
1.3.3 多肽的分离纯化
1.3.3.1 超滤
超滤法可以按照物料分子量大小的不同而对其进行初步的分离,分离的过程中工艺流程操作简单,所涉及到的化学试剂少,并且实验用时比较短[12]。将所得多肽粉先用适量的超纯水溶解,然后依次用截留分子量分别为 10000 u、5000 u 以及 3000 u 的超滤膜对所得到的四种酶解多肽进行初级分离,超滤过程中控制 CO2的压力使其少于 0.25 MPa,将超滤所得组分冻干,MTT 法测量其抗癌活性。
1.3.3.2 Sephadex G-15 分子筛层析[13]
填料预处理:将所需的凝胶填料粉末倒入烧杯中,加入适量的超纯水,置于电炉上煮沸 2h,加热期间用玻璃棒不断的搅拌,然后在室温下冷却,并放置12 h 使其溶胀充分。倒掉上层的水溶液和漂浮的细小颗粒,再用蒸馏水反复洗涤,至液面无悬浮的颗粒杂质。
装柱:选取规格为 2.6×40 cm 的玻璃柱,洗净,竖直固定在铁架台上,出口接上乳胶管,整个装置与蠕动泵连接,并在柱底部放置与口径相近的滤纸片,往玻璃柱中加入体积约为柱体积的 1/3 的超纯水,打开蠕动泵阀门,使水流通过从而排出装置内气泡,将预处理好的 Sephadex G-15 填料混匀,沿玻璃棒缓慢倒入,这一过程严禁柱子内气泡的产生(若有气泡需要重新装柱),装柱完毕最后保留的液面高度为 2~3 cm,在柱床上方覆盖一块同样小的滤纸片,以保持柱床表面的平整减缓外界对柱床的冲击,连接进水口,然后用超纯水平衡 2~3 个柱体积,至液面高度不再发生变化。
上样:将待分离的多肽用超纯水配置成浓度为 50 mg/m L,取 1 m L 上样,打开蠕动泵开关调整液面高度为 1 cm 左右,用吸管吸取样品在贴近液面处缓慢加入,最后加超纯水恢复为原来的液面高度,待样品完全渗入柱床内,开始收集。
洗脱收集:用超纯水进行洗脱,控制洗脱流速为0.3 m L/min,每管收集为 4 m L,用紫外分光光度计分别在 218 nm、274 nm 处测其吸光值。
1.3.4 MTT 法[14]测定多肽抗肿瘤细胞实验
选择活力较好的对数期生长细胞,加入 1 m L 的胰酶进行消化,在显微镜下观察到细胞形态变圆、细胞之间的间隙变大时,加入培养液 3 m L 终止消化,并用枪头吸取瓶内液体反复吹洗培养瓶底面制成细胞悬浮液。
用血球计数板进行计数,调节细胞液浓度为 5000个/100 µL,接种于 96 孔板上,每孔 100 µL,在 37 ℃细胞培养箱中培养24 h使细胞充分贴壁,吸出培养液,加 200 µL 含有不同多肽浓度的 DMEM 培养液,每个实验平行做 5 个孔,阴性对照为 DMEM 培养基,阳性对照为 5-氟尿嘧啶,继续在培养箱内培养 48 h,吸出含有多肽的培养液后用 PBS 进行洗涤,每孔加入 5 mg/m L 的 MTT20 µL 和 180 µL 的 DMEM 培养液,置于培养箱 4 h 后,吸出孔内液体,每孔中加 150 µL 的DMSO,在摇床上震荡 15 min,在 490 nm 下测 OD 值。
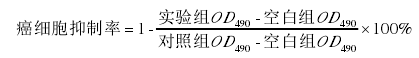
1.3.5 数据分析
所有数据均用 Origin 9.0 软件处理,除了 IC50采用软件中非线性拟合得出外,其余结果全部用平均值±标准偏差表示。
2 结果分析
2.1 蛋白含量测定结果
通过凯式定氮法测得金钱龟肉糜中的蛋白质含量为 14.70%。
2.2 蛋白水解度测定结果
胰蛋白酶水解度 30.57%,碱性蛋白酶水解度28.52%,木瓜蛋白酶水解度 17.29%,复合蛋白酶protamex 水解度 6.35%。
2.3 超滤所得不同分子量的酶解多肽对癌细胞的抑制效果
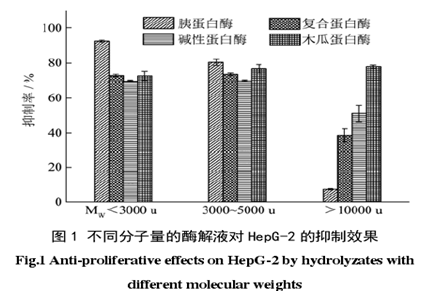
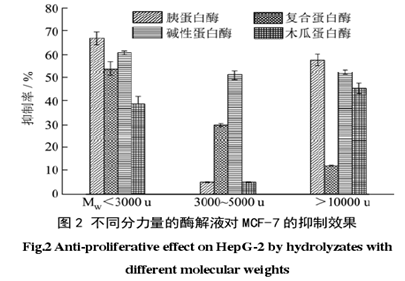
将四种酶解液依次用 10000 u、5000 u 和 3000 u的膜超滤后,每种酶解液都得到了分子量范围分别为0~3 000 u、3000~5000 u 和大于 10000 u 的酶解液(由于实验样品和酶解程度的原因 4次平行酶解超滤实验过程并中未得到 5000~10000 u 的组份),共计 12 种。将各酶解液冻干所得的多肽粉末用 DMEM 配制成浓度为 1 mg/m L 的溶液,用 MTT 法分别测试其对Hep G-2(如图 1)和 MCF-7(如图 2)两种癌细胞的抑制效果。
由图 1 和图 2 可知各不同分子量的酶解液对两种癌细胞均有一定的抑制作用,且整体来看绝大多数的酶解液对 Hep G-2 的抑制效果要强于 MCF-7。此外,当浓度相同时,不同的酶解液对癌细胞的抑制效果也不相同,通过对比发现胰蛋白酶酶解产物分子量为0~3000 u 的组分(设为组份 E)对两种癌细胞的抑制作用最强,对 Hep G-2 的抑制率为 92.95%,MCF-7 的抑制率为 67.08%,因此选择 E 进行下一步的分离纯化实验。
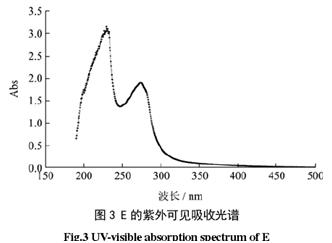
2.4 组分 E 的紫外光谱分析
由图 3可知,组分 E 主要呈现出两大较强紫外吸收峰,两吸收峰所对应的峰值分是218 nm 和 274 nm,因此选用这组数值做为后续分离液的紫外检测波长。
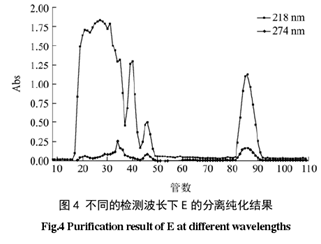
2.5 Sephadex G-15 分子筛层析
由上图可以看出,组分 E 经 Sephadex G-15 分离纯化时,当分离液的检测波长为218nm时,其效果要好于 280nm,故选择218nm为紫外检测波长。E经纯化后得到 4 个组份,分别为 E1、E2、E3 和 E4,将 4 组份冷冻干燥后保存备用。
2.6 E 的柱层析产物对癌细胞的抑制效果
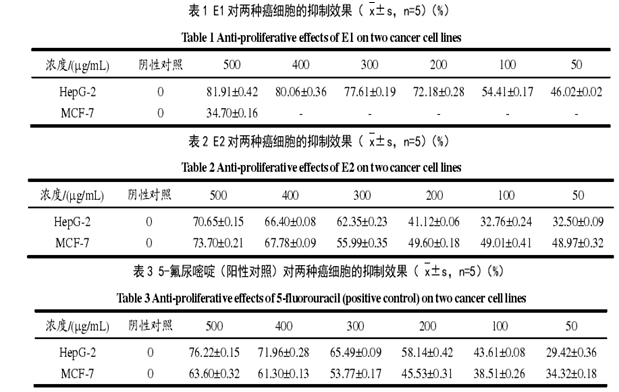
将 E1、E2、E3 和 E4 溶于 DMEM 配制成浓度为500 µg/m L 的溶液,采用 MTT 试验方法测得 4 组份对Hep G-2 和 MCF-7 两种癌细胞的抑制效果如图 5。由图 5可知 E1 对人肝癌细胞(Hep G-2)的抑制作用比较强,抑制率达到了 89.10%。E2 对人肝癌细胞(Hep G-2)和乳腺癌细胞(MCF-7)的抑制作用都比较显著,抑制率分别达到了 70.65%和 73.70%。将E1、E2 和阳性对照 5-氟尿嘧啶配制成梯度浓度:500µg/m L、400 µg/m L、300 µg/m L、200 µg/m L、100 µg/m L和 50 µg/m L,分别测得其对两种癌细胞的抑制率(见表 1~表 3),用 Origin 9.0 求得各组的 IC50值(见表 5)
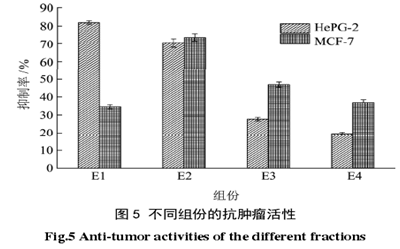
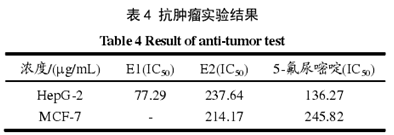
由表 1~表 4 可知 E1 对 Hep G-2 有显著的抑制作用,并且抑制率与浓度成正相关,通过与阳性对照半抑制浓度比较,说明其对 Hep G-2 抑制效果要强于阳性对照。E2 对 Hep G-2 和 MCF-7 均表现出了抑制作用,抑制率同样与浓度成正相关,通过与阳性对照半抑制浓度的比较,说明 E2 对 Hep G-2 抑制效果要低于阳性对照,E2 对 MCF-7 抑制效果要强于阳性对照。
3 结论
本研究以金钱龟为原料,以癌细胞的体外抑制实验(MTT)为筛选条件,结合分离纯化体系最终获得抗肿瘤活性肽。本研究得出以下结论:通过 4 种不同酶酶解结合超滤的初步纯化,得到 12 种酶解液组份,这 12 种组份的 MTT 实验结果显示胰蛋白酶酶解所得分子量小于 3000 u 的组份(设为 E)抗癌活性最强,当其浓度为 1 mg/m L 时,对 Hep G-2 和 MCF-7 的抑制率分别为 92.95%和 67.08%。E 经过 Sephadex G-15 进一步纯化得 4 组份 E1、E2、E3 和 E4,MTT 实验得出:E1 对 Hep G-2 的 IC50为 77.29 µg/m L,其抗癌效果要强于阳性对照 5-氟尿嘧啶(IC50为 136.27 µg/m L);E2 对 MCF-7 的 IC50为 214.17 µg/m L,其抗癌效果同样要强于阳性对照 5-氟尿嘧啶(IC50为245.82 µg/m L)。
参考文献
[1] 钟耀广.功能性食品[M].北京:化学工业出版社,2004
ZHONG Guang-Yao. Functional Food [M]. Bei Jing: Chemical Industry Press, 2014
[2] Picot L, Bordenave S, Didelot S, et al. Antiproliferative activity of fish protein hydrolysates on human breast cancer cell lines [J]. Process Biochemistry, 2006, 41(5): 1217-1222
[3] Bo Leng, Xiao-Dan Liu, Qing-Xi Chen. Inhibitory effects of anticancer peptide from Mercenaria on the BGC-823 cells and several enzymes [J]. FEBS Letters, 2005, 579(5): 1187- 1190
[4] 杨永芳,丁国芳,杨最素,等.紫贻贝酶解多肽体外抗肿瘤活性研究[J].浙江海洋学院学报(自然科学版),2011,30(2): 113-115
YANG Yong-fang, DING Guo-fang, YANG Zui-su, et al. The anticancer activityof peptide from hydrolysates of mytilusedulis [J]. Journal of Zhejiang Ocean University (Natural Science), 2011, 30(2): 113-115
[5] 姚如勇,初晓,陈守国,等.海洋泥蚶多肽抗肿瘤作用的实验研究[J].中国药学杂志,2006,41(11):868-870
YAO Ru-yong, CHU Xiao, CHEN Shou-guo, et al. Antitumor effects of polypeptides from arcagrano salinnaeusinvitro and in vivo [J]. Chin. Pharm. J., 2006, 41(11): 868-870
[6] Jumeri, Sang Moo Kim. Antioxidant and anticancer activities of enzymatic hydrolysates of solitary tunicate (Styelaclava) [J]. Food Sci. Biotechnol., 2011, 20(4): 1075- 1085
[7] 陈艳辉,李超柱,黎丹戎,等.动物蛋白酶酶解制备广西产牡蛎肉抗肿瘤活性肽的实验研究[
J].食品工业科技,2010, 8(31):167-169
CHEN Yan-hui, LI Chao-zhu, LI Dan-rong, et al. Experimental research on animal proteasome enzymatic hydrolysis for preparing antitumor bioactive peptide from oyster of Guangxi province [J]. Science and Technology of Food Industry, 2010, 8(31): 167-169
[8] Woo-Shin Lee, Joong-Kyun Jeon, Hee-Guk Byun. Characterization of a novel antioxidative peptide from the sand eel Hypoptychus dybowskii [J]. Process Biochemistry, 2011, 46(5): 1207-1211
[9] Raghavan S, Kristinsson H G. ACE-inhibitory activity of tilapia protein hydrolysates [J]. Food Chemistry, 2009, 117(4): 582-588
[10] Rim Nasri, Ikram Ben Amor, Ali Bougatef, et al. Anticoagulant activities of goby muscle protein hydrolysates [J]. Food Chemistry, 2012, 133(3): 835-841
[11] 华耀祖.超滤技术与应用[M].北京:化工工业出版社,2004
HUA Yao-Zu. Ultrafiltration Technology and Application[M]. Bei Jing: Chemical Industry Press, 2004
[12] Mei DJ, Yu GP, Sun AM. Preparation, purification and identification of antioxidant peptides with bienzyme hydrolysis from rice bran protein [C] // Progress In Environmental Science And Engineering. Jilin, PEOPLES R CHINA:Advanced Materials Research , 2013, 72-80
[13] Klucar J, Al-Rubeai M. G2 cell cycle arrest and apoptosis are induced in Burkitt’s lymphoma cells by the anticancer agent oracin [J]. FEBS Lett, 1997, 400(1): 127-130
收稿日期:2014-12-29
基金项目:国家 863 科技计划项目子课题(2014AA022004)
作者简介:何胜洁(1990-),女,硕士,从事抗癌功能食品研究
通讯作者:张学武(1963-),男,博士,教授,主要从事抗癌功能食品研究














